Forskel mellem alifatiske og aromatiske aminer | Alifatisk vs Aromatisk Aminer
Alifatisk vs Aromatisk Aminer
Den bedste og mest signifikante forskel mellem alifatiske og aromatiske aminer er den strukturelle forskel mellem de to forbindelser. Alifatiske aminer er aminforbindelserne, hvori nitrogen er bundet til kun alkylgrupper, og aromatiske aminer er aminforbindelserne, hvori nitrogen er bundet til mindst en af arylgrupperne. Denne strukturelle forskel fører til alle andre forskelle i deres egenskaber såsom reaktivitet, surhed og stabilitet.
Hvad er alifatiske aminer?
I alifatiske aminer bindes nitrogen direkte til kun alkylgrupper og hydrogenatomer . Antallet af alkylgrupper varierer fra en til tre. Afhængigt af antallet af vedhæftede alkylgrupper kaldes de " primære aminer " (kun en alkylgruppe -1 o ), " sekundære aminer " (to alkylgrupper - 2 o ) og " tertiære aminer " (tre alkylgrupper - 3 o ).
Alle alifatiske aminer er svage baser som ammoniak, men de er lidt stærkere baser end ammoniak. De har alle næsten den samme basestyrke Pkb = 3-4. Grundlæggende stigninger, idet hydrogengrupperne på nitrogenatomer erstattes af alkylgrupper. Tertiære aminer er mere grundlæggende end primære og sekundære aminer.
Når nitrogen er et af atomerne i en ring, kaldes de heterocykliske aminer . Piperidin og Pyrollidin er to eksempler for alifatiske heterocykliske aminer.
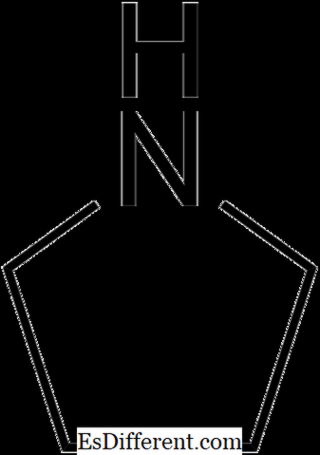
Pyrollidin
Hvad er aromatiske aminer?
I aromatiske aminer er nitrogen tilsat direkte til mindst en benzenring . Afhængigt af antallet af grupper, der er knyttet til nitrogenatomet, kategoriseres de som "primære", "sekundære" og "tertiære" aminer. " Aryl aminer " er et andet navn for aromatiske aminer. På samme måde som alifatiske aminer kan primære og sekundære aromatiske aminer danne intermolekylære hydrogenbindinger. Kogepunkter af primære og sekundære aminer er derfor relativt højere end de tertiære aminer.
Der er heterocykliske aromatiske aminer ; pyrrol og pyrydin er to eksempler for dem.

Pyrydine
Hvad er forskellen mellem alifatiske og aromatiske aminer?
• Struktur:
• Alkylaminer indeholder ikke benzenringe, der er direkte knyttet til nitrogenatomer.
• Men i aromatiske aminer er der mindst en benzenring, der er direkte knyttet til nitrogenatomet.
• Alifatiske aminer kan have aromatiske ringe, så længe nitrogen er direkte bundet til et carbonatom.
• Grundlæggende:
• Alifatiske aminer er stærkere baser end aromatiske aminer. Dette skyldes i grunden stabiliteten af den kation, der dannes efter ioniseringen. Med andre ord er alkylammoniumioner mere stabile end arylammoniumioner. Fordi alkylgrupper er elektronfrigivende grupper og således delokaliserer den positive ladning på nitrogenatomet.

• Alifatiske heterocykliske aminer er også stærkere baser end aromatiske heterocykliske aminer.
• Eksempler
• Eksempler på alifatiske heterocykliske aminer er Piperidin og Pyrollidin.
• Eksempler på heterocykliske aromatiske aminer er pyrrol og pyrydin.
Billeder Hilsen: Pyrollidin og Pyridin via Wikicommons (Public Domain)




