Forskel mellem Alkali Metaller og Alkaliske Jord Metaller | Alkali Metaller vs Alkaliske Jord Metaller
Alkalimetaller vs alkaliske jordmetaller < Da både alkalimetaller og jordalkalimetaller er de to første grupper i det periodiske bord, er forskellen mellem alkalimetaller og jordalkalimetaller et emne af interesse for enhver kemielever. Alkalimetaller og jordalkalimetaller kaldes også "S-blok" -elementerne, fordi elementer i begge disse grupper har deres yderste elektron (er) i s-subshell.
Generelt brugte vi ordet "metal" til de materialer, der fører elektricitet; både alkalimetaller og jordalkalimetaller er gode elektriske og varmeledere. Elementerne i disse to grupper er de mest reaktive metaller i det periodiske bord. Deres smeltepunkter er forholdsvis lave sammenlignet med andre metaller. Alkalimetaller og jordalkalimetaller har mange lignende egenskaber, men denne artikel omhandler hovedsageligt deres forskelle.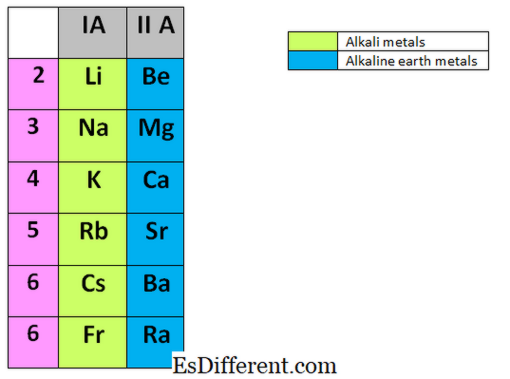
Alkalimetallerne er de elementer, der findes i den første gruppe i det periodiske bord. De er lithium (Li), Natrium (Na), Kalium (K), Rubidium (Rb), Cæsium (Cs) og Francium (Fr). De er alle metaller og meget reaktive, og ingen af disse metaller forekommer ikke som frie metaller i naturen. Alkalimetaller opbevares altid i inerte væsker som petroleum, fordi de hurtigt reagerer med luften, vanddampen og ilt i luften. Sommetider reagerer de eksplosivt med andre stoffer. De kan let opnå den ædle gasstilstand ved at fjerne den yderste elektron i valensskallen.
Tæthederne af lithium og natrium er mindre end vandtætheden. Imidlertid er de andre elementer tættere end vand. Mange af alkalimetalforbindelser (NaCl, KCl, Na 2 CO3, NaOH) er kommercielt meget vigtige. Hvad er alkaliske jordmetaller?
Alkaliske jordmetaller findes i den anden gruppe af det periodiske bord. Gruppe II-elementer omfatter; Beryllium (Be), Magnesium (Mg), Calcium (Ca), Strontium (Sr), Barium (Ba) og Radium (Ra). På samme måde som alkaliske metaller, forekommer disse elementer heller ikke frit i naturen, og de er også meget reaktive.
Alle elementerne i denne gruppe er tættere end vand. Rene metaller er sølvgråfarvede, men de har tendens til at affarve hurtigt, når de udsættes for luft, fordi de danner et oxidlag på overfladen. Ligesom alkalimetaller er disse metaller også gode ledere i varme og elektricitet.Alle jordalkalimetaller er kommercielt værdifulde.
Hvad er forskellen mellem alkalimetaller og alkaliske jordmetaller?
Elektronkonfiguration
- : Alkalimetaller har den elektroniske konfiguration af [Noble gas] ns 1 og jordalkalimetaller har [Noble gas] ns 2 elektronisk konfiguration. Valence
- : Alle alkalimetaller har en elektron i deres yderste skal, og alle jordalkalimetaller har to ydre elektroner. For at opnå ædelgaskonfigurationen skal alkalimetaller tabe en elektron (valens er "en"), mens jordalkalimetaller skal fjerne to elektroner (valens er "to"). Reaktivitet
- : Både alkalimetaller og alkalimetaller er meget reaktive. Alkalimetaller er mere reaktive end jordalkalimetaller. Jonisk ladning
- : Alkalimetaller har 1 ionisk ladning i deres forbindelser, og jordalkalimetaller har +2 ionladning i forbindelser. Hårdhed
- : Alkalimetaller er meget bløde og kan skæres med en skarp kniv. Alkaliske jordmetaller er sværere end alkalimetallerne. Sammendrag:
Alkalimetaller vs alkaliske jordmetaller




