Forskel mellem Thomson og Rutherford Model of Atom | Thomson vs Rutherford Model of Atom
Nøgleforskel - Thomson vs Rutherford Model af Atom
Hovedforskellen mellem Thomson og Rutherford-modellen af atom er, at Thomson-modellen af atom indeholder ingen detaljer om kernen mens Rutherford-model af atom forklarer om kernen af et atom. J. J. Thomson var den første til at opdage den subatomære partikel kaldet elektron i 1904. Den model, han foreslog, blev benævnt "plumpudding-model af atomet". Men i 1911 kom Ernest Rutherford op med en ny model for atomet efter sin opdagelse af atomkernen i 1909.
INDHOLD
1. Oversigt og nøgleforskel
2. Hvad er Thomson Model of Atom
3. Hvad er Rutherford Model of Atom
4. Side om side Sammenligning - Thomson vs Rutherford Model af Atom i Tabular Form
5. Sammendrag
Hvad er Thomson Model of Atom?
Thomson-modellen af atom kaldes Plum pudding model fordi det hedder at atomet ligner en blommepudding. De eneste kendte detaljer om atom på det tidspunkt var,
- Atomer er sammensat af elektroner
- Elektroner er negativt ladede partikler
- Atomer er neutralt opladede
Da elektroner er negativt ladede, foreslog Thomson, at der skulle være en positiv ladning for at neutralisere den elektriske ladning af atomet. Thomson-modellen af atom forklarer, at elektroner er indlejret i et positivt ladet fast materiale, der er kugleformet. Denne struktur ligner en pudding med blommer indlejret på den og blev opkaldt som plum pudding model af atom. Dette viste, at antagelsen om at et atom er neutralt ladet, da denne model angiver, at de negative ladninger af elektroner neutraliseres af den positive ladning af den faste kugle. Selv om denne model viste, at atomer er neutralt ladet, blev det afvist efter opdagelsen af kernen.

Figur 01: Thomson Model of Atom
Hvad er Rutherford Model of Atom?
Ifølge Rutherford-modellen af atom var den såkaldte Plum Pudding-model af Thomson ukorrekt. Rutherford-model af atom kaldes også nuklearmodel , fordi den giver detaljer om kernen i et atom.
Det berømte eksperiment kaldet "Rutherford Gold Foil Experiment" førte til opdagelsen af kernen. I dette eksperiment blev alfa-partikler bombarderet gennem en guldfolie; de forventedes at gå lige igennem guldfolien. Men i stedet for lige indtrængning forvandlet alfa-partikler til forskellige retninger.
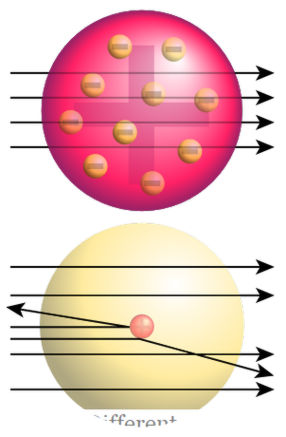
Figur 02: Rutherford Gold Foil Experiment Top: Forventede resultater (lige indsnævring) Nederste : Observerede resultater (afbøjning af nogle partikler)
Dette viste at der er noget solidt med en positiv ladning i den guldfolie, der forårsager en kollision med alfa partikler. Rutherford hedder denne positive kerne som kernen. Derefter foreslog han kernemodellen for atomet; den var sammensat af en positivt ladet kerne og negativt ladede elektroner omkring kernen. Han foreslog også, at elektroner er i orbitaler omkring kernen i visse afstande. Denne model kaldes også planetarisk model , fordi Rutherford foreslog, at elektroner er placeret rundt om kernen ligner planeterne, der ligger omkring solen.
Ifølge denne model er
- Atomet sammensat af et positivt ladet center, der kaldes kernen. Dette center indeholdt atomets masse.
- Elektroner er placeret uden for kernen i orbitaler i en betydelig afstand.
- Antallet af elektroner er lig med antallet af positive ladninger (senere kaldet protoner) i kernen.
- Kernens volumen er ubetydelig i forhold til atomets volumen. Derfor er det meste af rummet i atomet tomt.
Denne Rutherford-model af atom blev imidlertid afvist, fordi den ikke kunne forklare, hvorfor elektronerne og de positive ladninger i kernen ikke tiltrækkes til hinanden.

Figur 03: Rutherford Model of Atom
Hvad er forskellen mellem Thomson og Rutherford Model of Atom?
Thomson vs Rutherford Model af Atom
Thomson-model af atom er modellen, der siger at elektroner er indlejret i et positivt ladet fast materiale, som er kugleformet. |
|
| Rutherford-model af atom er modellen, der forklarer, at der er en kernen i atomets centrum, og elektroner er placeret omkring kernen. | Nucleus |
| Thomson-model af atom giver ikke nogen detaljer om kernen. | |
| Rutherford-model af atom giver detaljer om kernen af et atom og dets placering inde i atomet. | Placering af elektroner |
| Ifølge Thomson-modellen af atom er elektroner indlejret i et fast materiale. | |
| Rutherford-modellen siger, at elektroner er placeret rundt om kernen. | Orbitaler |
| Thomson-model af atom giver ikke detaljer om orbitaler. | |
| Rutherford-model af atom forklarer om orbitaler, og at elektroner er placeret i disse orbitaler. | Masse |
| Thomson-modellen af atom forklarer at massen af et atom er massen af positivt ladet faststof, hvor elektroner er indlejret. | |
| Ifølge atommodellen Rutherford er massen af et atom koncentreret i atomets kernen. | Sammenfatning - Thomson vs Rutherford Modeller af Atom |
Thomson og Rutherford-modeller af atom var de tidligste modeller til at forklare et atoms struktur. Efter J. J. Thomsons opdagelse af elektronen foreslog han en model for at forklare atomets struktur. Senere opdagede Rutherford kernen og introducerede en ny model ved hjælp af både elektron og kerner. Den væsentligste forskel mellem Thomson og Rutherford-modellen af atom er, at Thomson-modellen af atom ikke indeholder nogen detaljer om kerner, mens Rutherford-model af atom forklarer kernens atom.
Download PDF Version af Thomson vs Rutherford Modeller af Atom
Du kan downloade PDF-versionen af denne artikel og bruge den til offline-formål som i citatnotater. Venligst download PDF version her Forskellen mellem Thomson og Rutherford Model of Atom.
Reference:
1. "Rutherford Model of the Atom: Definition & Diagram. " Undersøgelse. com. n. d. Web. Tilgængelig her. 06 juni 2017.
2. Brescia, Frank. Grundlag for kemi: En moderne introduktion (1966). Elsevier, 2012. Udskriv.
3. Goldsby, Kenneth. Kemi. 12. udgave. New York: McGraw-Hill, 2015. Udskriv.
Image Courtesy:
1. "Plum pudding atom" (Public Domain) via Commons Wikimedia
2. "Rutherford atom" Ved eget arbejde (CreateJODER Xd Xd) (CC BY-SA 3. 0) via Commons Wikimedia
3. "Rutherford Gold Foil Experiment Resultater" Af Bruger: Fastfission Egent arbejde (Public Domain) via Commons Wikimedia




